L'atome d'hélium complètement ionisé He++ ( manquent les deux électrons) est aussi dénommé "particule alpha" (voir la section histoire. Dans le soleil et la plupart des étoiles, l'hydrogène est l'élément le plus abondant avec l'hélium , le suivant. Donc le vent solaire est avant tout constitué de protons, avec 5% de particules alpha et un nombre restreint d'ions plus lourds.
Les rayons cosmiques ont une composition assez semblable : il s'agit d'un voile très mince d'ions, se déplaçant presque à la vitesse de la lumière, qui bombardent la terre en toutes directions ; ils sont probablement présents dans toute notre galaxie mais leur origine est incertaine. .
Il faut dire qu'en plus de ces ions "atomiques", il existe aussi des ions moléculaires d'un signe ou de l'autre, se formant lorsqu'une molécule intacte perd ou gagne un électron. Cela se produit en particulier dans les processus ionosphériques.
Nuages ionisés du baryum
Un atome peut s'ioniser par absorption de lumière. l'atome du baryum s' ionise particulièrement facilement, parce que son électron extérieur est très faiblement lié. Si dans l'espace une masse de baryum tourne à l'état de vapeur, devenant un nuage de baryum, en moins d'une minute la plus grande partie de celle-ci s'ionise sous l'effet de la lumière du soleil. Le nuage se déplace alors en réponse aux forces électriques de l'espace, et on peut en profiter pour étudier le champ électrique de celui-ci.
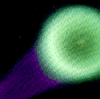
En pratique le baryum est enfermé avec de l'oxyde de cuivre dans des boîtes métalliques, qui sont libérées à partir des fusées ou des satellites mis à feu. Il en résulte une réaction chimique et une grande chaleur, mais il y a du baryum en excès dans la boîte métallique dont une partie est vaporisée et forme un grand nuage sphérique et verdâtre.
 Normalement cette libération est effectuée juste après le coucher du soleil ou juste avant le lever du soleil, pour que les boîtes métalliques éclatent en pleine lumière du soleil et que les observateurs sur la terre puissent observer le nuage sur fond de ciel foncé : ils observent bientôt un nuage d'ion bleuâtre distinct d'un nuage vert, habituellement allongé dans la direction des lignes de champ magnétique, qui guident les ions.
Normalement cette libération est effectuée juste après le coucher du soleil ou juste avant le lever du soleil, pour que les boîtes métalliques éclatent en pleine lumière du soleil et que les observateurs sur la terre puissent observer le nuage sur fond de ciel foncé : ils observent bientôt un nuage d'ion bleuâtre distinct d'un nuage vert, habituellement allongé dans la direction des lignes de champ magnétique, qui guident les ions.

La Composition En Charge d'AMPTE
satellite Explorer(CCE)
Quelques tirs de baryum ont eu lieu loin de la terre et ont été suivis au télescope. La mission AMPTE (Active Magnetospheric Particle Tracer Experiment), lancée en 1984, a libéré des nuages de baryum près du "nez" de la magnétosphère et dans sa queue. La mission AMPTE utilisait trois vaisseaux spatiaux, montré ici "empilés" pendant le lancement. Cliquez ici pour une version normale de cette image. De plus elle a libéré un nuage de baryum dans le vent solaire pour produire "une comète artificielle". Peu après que la formation du nuage, le champ magnétique du vent solaire l'a pris en charge et l'a orienté dans sa direction, un processus semblable à celui qui crée les queues ioniques des comètes (voir le vent solaire, l'histoire).
.
Questions des lecteurs (anglaise):
.
***